Avances en psiquiatría de precisión y medicina personalizada: Un análisis integral de la farmacogenómica, los biomarcadores moleculares y el fenotipado digital
La evolución del paradigma: Del diagnóstico descriptivo a la medicina basada en mecanismos
La psiquiatría se encuentra en el umbral de una transformación histórica que busca trascender las limitaciones inherentes a los sistemas de clasificación tradicionales. Durante gran parte del siglo XX y principios del XXI, la disciplina se ha cimentado en un modelo descriptivo y sindrómico, ejemplificado por el Manual Diagnóstico y Estadístico de los Trastornos Mentales (DSM-5) y la Clasificación Internacional de Enfermedades (CIE-11). Si bien estos marcos han facilitado la comunicación clínica y la estandarización de la investigación, carecen de una base fisiopatológica sólida, lo que genera una heterogeneidad biológica masiva dentro de una misma categoría diagnóstica. Esta brecha es la causa fundamental de lo que se denomina el «dilema de la imprecisión», donde el tratamiento de primera línea para trastornos como la depresión mayor o la esquizofrenia sigue siendo, en gran medida, un proceso de ensayo y error con tasas de remisión inicial que apenas alcanzan el 30%.
La medicina personalizada en psiquiatría, o psiquiatría de precisión, propone un enfoque dinámico que integra datos biológicos, clínicos y ambientales para adaptar la intervención a las características únicas de cada individuo. Este paradigma no se limita únicamente a la farmacogenómica; abarca un ecosistema que incluye la neuroinflamación, la neuroplasticidad, el microbioma intestinal, el fenotipado digital y el aprendizaje automático para predecir trayectorias de enfermedad y optimizar la selección de fármacos. La evidencia acumulada hasta 2025 sugiere que la integración de estos dominios permite una estratificación de riesgo mucho más fina, permitiendo al clínico actuar sobre los circuitos neuronales específicos que subyacen a la sintomatología del paciente.

Fundamentos neurocientíficos de la neurotransmisión química y la plasticidad
Para comprender la medicina personalizada, es imperativo profundizar en la base de la psicofarmacología moderna: la neurotransmisión química. Según el marco conceptual de Stephen Stahl, la neurotransmisión no debe visualizarse simplemente como una neurona presináptica comunicándose con una postsináptica a través de un neurotransmisor, sino como una conversación compleja entre genomas. Este proceso se describe mediante tres rutas secuenciales denominadas «molecular pony express»: la ruta de síntesis presináptica, la ruta postsináptica de segundos mensajeros que activa genes, y la cascada molecular resultante de los genes recién expresados que altera la bioquímica de la neurona a largo plazo.
El objetivo final de cualquier tratamiento psiquiátrico personalizado es modificar estas cascadas moleculares para restaurar la función de los circuitos. Aquí, la epigenética juega un papel determinante. Los mecanismos epigenéticos —metilación del ADN, acetilación de histonas y modificaciones de la cromatina— funcionan como interruptores moleculares que activan o silencian genes en respuesta al ambiente, las drogas y el estrés. La variabilidad individual en estos perfiles epigenéticos explica por qué dos pacientes con la misma secuencia de nucleótidos pueden responder de manera diferente al tratamiento o mostrar vulnerabilidades distintas a los efectos secundarios.
El eje de la neuroplasticidad: GSK-3 y mTOR
La medicina de precisión moderna pone especial énfasis en enzimas involucradas en la transducción de señales y la supervivencia celular. La glucógeno sintasa quinasa 3 (GSK-3) ha emergido como una diana terapéutica fundamental, particularmente en el trastorno bipolar. Se ha postulado que el litio actúa inhibiendo la GSK-3, lo que promueve acciones neuroprotectoras y plasticidad sináptica a largo plazo. Identificar variantes genéticas o niveles de actividad en la vía de la GSK-3 podría permitir en un futuro predecir qué pacientes son «respondedores al litio» antes de iniciar un tratamiento de meses.
De igual manera, la vía de la diana de rapamicina en células de mamífero (mTOR) es crítica para la respuesta antidepresiva rápida. Fármacos como la ketamina y la esketamina ejercen sus efectos mediante la activación de mTOR, lo que conduce a una síntesis rápida de proteínas sinápticas y a la reversión de la atrofia dendrítica inducida por el estrés crónico. La capacidad de medir el «compromiso de diana» en estas vías intracelulares representa la frontera final de la personalización psicofarmacológica.
Farmacogenómica avanzada: De los genes candidatos a los puntajes poligénicos
La farmacogenómica (PGx) constituye el núcleo histórico de la medicina personalizada en psiquiatría. Su aplicación clínica se divide tradicionalmente en farmacocinética (qué hace el cuerpo con el fármaco) y farmacodinamia (qué hace el fármaco en el cerebro).
Farmacocinética y el sistema citocromo P450
La mayoría de los psicotrópicos son procesados por las enzimas del sistema citocromo P450 (CYP450), siendo CYP2D6 y CYP2C19 las más relevantes. Las variaciones genéticas en estos genes pueden clasificar a los pacientes en fenotipos que determinan la seguridad y eficacia del tratamiento. Por ejemplo, un paciente categorizado como metabolizador lento para CYP2D6 corre un riesgo elevado de toxicidad con dosis estándar de antidepresivos tricíclicos o ciertos antipsicóticos, mientras que un metabolizador ultrarrápido podría nunca alcanzar niveles plasmáticos terapéuticos, resultando en un fracaso del tratamiento mal interpretado como resistencia.

Farmacodinamia y polimorfismos específicos
La personalización dinámica se centra en las variaciones de los receptores y transportadores. Uno de los biomarcadores más debatidos es el polimorfismo 5-HTTLPR en el gen del transportador de serotonina (SLC6A4). El alelo corto (S) se ha asociado históricamente con una menor expresión del transportador y una respuesta menos favorable a los inhibidores selectivos de la recaptación de serotonina (ISRS) en individuos de ascendencia caucásica, además de un aumento de los efectos secundarios gastrointestinales. No obstante, la evidencia actual sugiere que estos marcadores deben interpretarse con cautela, ya que su efecto varía significativamente según la etnia y el sexo del paciente.
Otro marcador crítico es el gen BDNF, donde el polimorfismo Val66Met altera la secreción de este factor neurotrófico dependiente de la actividad neuronal. Los portadores del alelo Met muestran una plasticidad reducida, lo que se ha vinculado con una mayor vulnerabilidad al estrés y una respuesta más lenta a los antidepresivos convencionales.
La revolución de las puntuaciones de riesgo poligénico (PRS)
A diferencia de los estudios de genes candidatos únicos, las puntuaciones de riesgo poligénico (PRS) agregan el efecto de miles de variantes genéticas de efecto pequeño identificadas en estudios de asociación del genoma completo (GWAS). En 2025, los PRS han demostrado una capacidad modesta pero consistente para predecir la trayectoria clínica. Un PRS elevado para la depresión se correlaciona con una mayor probabilidad de no respuesta a múltiples clases de fármacos y un mayor riesgo de resistencia al tratamiento. Sin embargo, la implementación clínica de los PRS enfrenta barreras éticas y técnicas considerables, incluyendo la falta de diversidad genómica, ya que la mayoría de los modelos se basan en poblaciones de ascendencia europea, lo que limita su utilidad en poblaciones diversas.
Nomenclatura basada en la neurociencia (NbN): Un lenguaje para la precisión
La medicina personalizada requiere una terminología que refleje la realidad biológica de los fármacos. La nomenclatura tradicional, que clasifica a los medicamentos según su indicación clínica original (ej. «antidepresivos», «antipsicóticos»), es fuente de estigma y confusión para el paciente. Por ejemplo, un paciente con ansiedad puede mostrar resistencia a tomar un «antidepresivo», o un paciente con depresión resistente puede alarmarse si se le prescribe un «antipsicótico».
La NbN busca armonizar la psiquiatría con el resto de la medicina, clasificando los psicotrópicos según su diana molecular y su modo de acción. Este sistema identifica 11 dominios farmacológicos y 10 modos de acción, permitiendo al clínico realizar una selección racional basada en el circuito que desea modular.
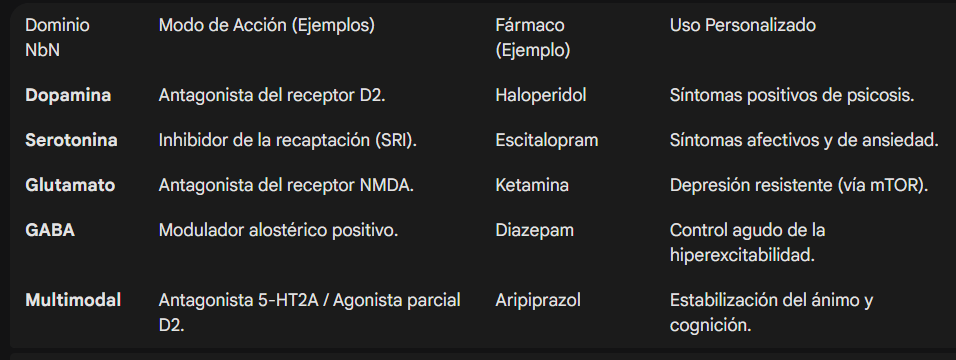
Esta transición hacia la NbN facilita la «psicofarmacología informada por circuitos», donde el clínico evalúa qué dimensiones psicopatológicas están afectadas (ej. afecto negativo, anhedonia, disfunción ejecutiva) y selecciona el agente con el perfil neuroquímico más adecuado, independientemente de la etiqueta diagnóstica clásica.
Inmunopsiquiatría: La inflamación como biomarcador de estratificación
Uno de los avances más prometedores en la personalización del tratamiento es el reconocimiento del papel de la inflamación sistémica en los trastornos mentales. Se estima que aproximadamente un tercio de los pacientes con trastorno depresivo mayor presentan niveles elevados de biomarcadores inflamatorios, un estado que a menudo se correlaciona con la resistencia a los tratamientos convencionales.
El papel de la PCR y las citoquinas proinflamatorias
La proteína C reactiva de alta sensibilidad (PCR-as), la interleucina-6 (IL-6) y el factor de necrosis tumoral alfa (TNF-$\alpha$) han emergido como indicadores críticos de la respuesta terapéutica. Niveles de PCR-as superiores a $3$ mg/L se asocian consistentemente con una respuesta deficiente a los ISRS. Estos pacientes, en cambio, pueden mostrar una mejor respuesta a antidepresivos con mecanismos noradrenérgicos o dopaminérgicos, o incluso a la adición de agentes antiinflamatorios como el infliximab en subgrupos específicos.

La vía de la quinurenina: El secuestro del triptófano
Un mecanismo central de la neuroinmunología es el desvío del metabolismo del triptófano inducido por la inflamación. En presencia de citoquinas proinflamatorias, la enzima indolamina 2,3-dioxigenasa (IDO) se activa, convirtiendo el triptófano en quinurenina en lugar de serotonina. La quinurenina se metaboliza posteriormente en ácido quinolínico, que es neurotóxico y activa los receptores NMDA, contribuyendo al daño neuronal y al deterioro cognitivo. La medicina de precisión busca identificar a estos pacientes para intervenir precozmente, ya sea mediante la reducción de la inflamación sistémica o el bloqueo de los efectos neurotóxicos de los metabolitos de la quinurenina.
Fenotipado digital y biomarcadores conductuales: Monitoreo en tiempo real
La medicina personalizada requiere datos continuos y objetivos que las evaluaciones clínicas intermitentes no pueden proporcionar. El fenotipado digital, mediante el uso de teléfonos inteligentes y dispositivos portátiles (wearables), ofrece una visión dinámica y contextualizada del estado mental del paciente.
Sensores pasivos y biomarcadores digitales
La recopilación de datos pasivos permite identificar desviaciones sutiles de la línea base del paciente que a menudo preceden a una recaída clínica. Estos datos incluyen:
- Movilidad (GPS): La reducción de la varianza en la ubicación y el aumento del tiempo en casa son predictores potentes de episodios depresivos.
- Actividad física (Acelerometría): Cambios en el ritmo circadiano y niveles de energía pueden detectar el inicio de una fase maníaca antes de que el paciente reporte síntomas.
- Uso del smartphone: La frecuencia de interacción, la velocidad de escritura y los patrones de comunicación social sirven como biomarcadores de la velocidad psicomotriz y la estabilidad afectiva.
Inteligencia Artificial (IA) en la selección del tratamiento
La IA y el aprendizaje automático (ML) son los catalizadores necesarios para procesar estas vastas cantidades de datos biológicos y digitales. Los modelos de ML pueden integrar registros electrónicos de salud, datos de neuroimagen y perfiles inflamatorios para predecir el riesgo de suicidio o la probabilidad de respuesta a un fármaco específico con precisiones que superan el 80%. Un avance reciente en 2025 es la utilización de modelos de lenguaje de gran tamaño (LLM) para interpretar datos de fenotipado digital, aunque este proceso aún requiere una supervisión humana estricta para evitar «alucinaciones» de datos o sesgos algorítmicos.
Microbioma y el eje intestino-cerebro: La frontera de la farmacomicrobiómica
El microbioma intestinal ha emergido como un regulador crítico de la salud cerebral, influyendo en la síntesis de neurotransmisores, la integridad de la barrera hematoencefálica y la regulación inmunológica. La farmacomicrobiómica estudia cómo las variaciones en la composición bacteriana pueden alterar el metabolismo de los fármacos psiquiátricos, influyendo en su biodisponibilidad y efectividad.
Investigaciones recientes han identificado taxones bacterianos específicos asociados con la depresión mayor. Los pacientes con TDM a menudo muestran una reducción en géneros productores de butirato, como Faecalibacterium y Roseburia, y un enriquecimiento de bacterias proinflamatorias como Alistipes. La personalización del tratamiento en este campo podría incluir la prescripción de «psicobióticos» —probióticos que confieren beneficios para la salud mental— o dietas personalizadas diseñadas para reducir la neuroinflamación mediada por el eje intestino-cerebro.
Etapificación clínica (Clinical Staging): Proporcionalidad y prevención
Para que la medicina de precisión sea efectiva, debe aplicarse en el momento adecuado de la progresión de la enfermedad. Inspirados en la oncología, los modelos de etapificación clínica en psiquiatría —liderados por Patrick McGorry— buscan clasificar los trastornos según su gravedad y trayectoria evolutiva.
El modelo de McGorry y la intervención temprana
Este modelo propone seis etapas (0 a 4), destacando la importancia de actuar en las fases prodrómicas (1a y 1b), donde los síntomas son inespecíficos pero el riesgo de progresión es alto. La etapificación permite aplicar el principio de proporcionalidad: intervenciones benignas y de bajo riesgo (psicoterapia, cambios de estilo de vida, omega-3) en etapas tempranas, y farmacoterapia intensiva o neuromodulación en etapas avanzadas de enfermedad crónica o refractaria.

Proyecto BOARDING-PASS: Un ejemplo de integración en el trastorno bipolar
El proyecto BOARDING-PASS representa la vanguardia de la etapificación biológicamente informada en 2025. Este estudio longitudinal integra perfiles clínicos, biomarcadores inflamatorios, firmas epigenéticas y datos de neuroimagen (conectoma funcional y estructural) para predecir la transición de los pacientes a través de las etapas del trastorno bipolar. Mediante algoritmos de ML, el proyecto busca identificar «biotipos» de progresión que permitan una prevención secundaria altamente personalizada.
Aplicaciones prácticas en subpoblaciones específicas
Medicina personalizada en la demencia y el envejecimiento
En el ámbito de los trastornos neurocognitivos, la personalización se centra en la gestión de los síntomas conductuales y psicológicos de la demencia (BPSD). Dado que los pacientes ancianos presentan cambios en la ratio grasa-músculo y una reducción en el aclaramiento renal y hepático, el principio de «empezar bajo e ir despacio» es fundamental. La personalización terapéutica incluye el uso de inhibidores de la acetilcolinesterasa para la memoria y nuevos agentes como la pimavanserina, que actúa selectivamente en los receptores 5-HT2A para tratar la psicosis en la enfermedad de Parkinson sin exacerbar los síntomas motores del bloqueo D2 convencional.
Precisión en los trastornos impulsivo-compulsivos y adicciones
El enfoque personalizado en las adicciones utiliza el conocimiento de los circuitos de recompensa y las señales de «pare» corticales. La farmacogenómica del receptor opioide mu (μ) puede ayudar a identificar a pacientes con mayor riesgo de recaída o aquellos que responderán mejor al bloqueo con naltrexona. Además, el uso de formulaciones de naltrexona de acción prolongada es una forma de personalización logística para pacientes con dificultades de adherencia, estabilizando los niveles plasmáticos y eliminando la necesidad de una decisión diaria sobre la toma del medicamento.
Barreras para la implementación y desafíos éticos
A pesar del potencial transformador de la psiquiatría de precisión, existen obstáculos significativos para su adopción masiva:
Costo y acceso: Las pruebas genómicas completas y el monitoreo digital avanzado siguen siendo inaccesibles para gran parte de la población mundial y a menudo no están cubiertos por los sistemas públicos de salud.
Privacidad de datos: El fenotipado digital plantea interrogantes críticas sobre quién posee los datos de comportamiento y cómo se protegen frente al uso comercial o discriminatorio por parte de aseguradoras y empleadores.
Sesgo algorítmico: Existe un riesgo real de que los modelos predictivos, entrenados mayoritariamente en poblaciones occidentales, perpetúen disparidades en el diagnóstico y tratamiento de minorías étnicas.
Complejidad para el clínico: La integración de flujos masivos de datos requiere herramientas de apoyo a la decisión clínica (CDSS) que sean intuitivas y no contribuyan al agotamiento profesional de los psiquiatras.
Recomendaciones para la optimización de la práctica clínica personalizada
La transición hacia una medicina de precisión exitosa requiere que el profesional de la salud mental evolucione de ser un observador pasivo de síntomas a un integrador activo de datos biológicos. Las siguientes estrategias son fundamentales para mejorar la precisión diagnóstica y terapéutica:
- Adopción de la NbN: Sustituir la nomenclatura basada en indicaciones por una basada en mecanismos moleculares para reducir el estigma y mejorar la adherencia del paciente.
- Integración juiciosa de la PGx: Utilizar las pruebas farmacogenéticas no como un oráculo definitivo, sino como una herramienta para ajustar dosis y predecir tolerabilidad, especialmente en casos de polifarmacia o respuestas atípicas.
- Evaluación del estado inflamatorio: Considerar la medición de la PCR-as y citoquinas en pacientes con depresión resistente para identificar a aquellos que podrían beneficiarse de estrategias inmunomoduladoras.
- Implementación de modelos de etapificación: Evaluar la etapa evolutiva del paciente para ofrecer intervenciones proporcionadas y enfocadas en detener la neuroprogresión.
- Uso del fenotipado digital: Aprovechar los datos de wearables y smartphones para un monitoreo proactivo que permita la detección temprana de crisis y el ajuste dinámico del tratamiento.
En conclusión, la medicina personalizada en psiquiatría ya no es una promesa futurista, sino una realidad en expansión que busca devolver la singularidad biológica y humana al centro de la práctica clínica. La integración de la genómica, la inmunología y la tecnología digital no solo mejorará los resultados terapéuticos, sino que permitirá una comprensión más profunda y compasiva de la complejidad del cerebro humano y sus trastornos.